Перейти к:
Оценка эффективности нейромодуляции у пациентов с фармакорезистентной эпилепсией после неудачного хирургического лечения
https://doi.org/10.17749/2077-8333/epi.par.con.2024.184
Аннотация
Актуальность. В ситуациях, когда консервативная противоэпилептическая терапия неэффективна, возможно хирургическое лечение, направленное на удаление эпилептогенного очага. Резекционные операции позволяют избавиться от приступов в большинстве случаев, однако у 20–30% больных они сохраняются или рецидивируют. В таких случаях пациентам может быть предложен тот или иной вид нейромодуляции.
Цель: оценка эффективности проведения нейромодуляции у пациентов с фармакорезистентной эпилепсией (ФРЭ) после неудачных резекционных хирургических вмешательств.
Материал и методы. Проведен ретроспективный анализ данных 23 пациентов, которым после неудачной операции по поводу ФРЭ проводилась стимуляция блуждающего нерва (англ. vagus nerve stimulation, VNS) либо глубокая стимуляция (англ. deep brain stimulation, DBS) переднего ядра таламуса (англ. anterior nucleus of the thalamus, ANT) или гиппокампа (англ. hippocampus, HP). Система VNS имплантирована 18 (78,3%) больным, система HP-DBS – 3 (13,0%), система ANT-DBS – 2 (8,7%). Результаты хирургических вмешательств оценивали по шкале Engel, VNS-терапии – по шкале McHugh (MH), DBS-терапии – по степени снижения частоты приступов в процентах. Средний катамнез наблюдения составил 56,5 мес.
Результаты. В группе пациентов, которым была имплантирована система VNS, у 3 (16,7%) исход составил MH Ia–IIb, у 10 (55,5%) – MH IIIa–IIIb, у 5 (27,8%) – MH IV–V. В группе HP-DBS у 2 больных из 3 отмечено снижение частоты приступов более чем на 50% от исходного уровня, у 1 пациента наблюдалось облегчение тяжести приступов. В группе ANT-DBS у одного больного зарегистрировано снижение частоты приступов на 60% и облегчение тяжести приступов, у второго изменений в частоте приступов не отмечено.
Заключение. Нейромодуляция у пациентов с ФРЭ позволяет значимо уменьшить частоту приступов у более чем половины пациентов после неудачного оперативного лечения.
Ключевые слова
Для цитирования:
Ефремов Ф.А., Агаев Р.В., Ким С.А., Мойсак Г.И., Анисимов Е.Д., Хабарова Е.А., Рзаев Д.А. Оценка эффективности нейромодуляции у пациентов с фармакорезистентной эпилепсией после неудачного хирургического лечения. Эпилепсия и пароксизмальные состояния. 2024;16(2):96-103. https://doi.org/10.17749/2077-8333/epi.par.con.2024.184
For citation:
Efremov F.A., Agaev R.V., Kim S.A., Moisak G.I., Anisimov E.D., Khabarova E.A., Rzaev J.A. Effectiveness of neuromodulation in patients with drug-resistant epilepsy after failed surgical treatment. Epilepsy and paroxysmal conditions. 2024;16(2):96-103. https://doi.org/10.17749/2077-8333/epi.par.con.2024.184
ВВЕДЕНИЕ / INTRODUCTION
По меньшей мере 50 млн человек во всем мире страдают эпилепсией, и до 40% из них – фармакорезистентной эпилепсией (ФРЭ). ФРЭ часто протекает тяжело и приводит к инвалидизации, а также связана со смертностью в 5–10 раз выше, чем в общей популяции. Риск преждевременной смерти у больных эпилепсией почти в 3 раза превышает средний показатель по популяции [1][2].
Резекционные операции при ФРЭ обладают высокой эффективностью и в большинстве случаев позволяют добиться полного избавления от приступов. Однако радикальные хирургические вмешательства не показаны пациентам с ФРЭ в случаях с двусторонней или распространенной эпилептической активностью при расположении зоны эпилептогенного очага вблизи функционально значимых зон, а также при невозможности определения локализации зоны начала приступа. Кроме того, у 20–30% пациентов после резективного хирургического вмешательства приступы сохраняются [3]. В этих случаях можно говорить о неудаче проведенной операции.
В настоящее время таким пациентам кроме коррекции противоэпилептической терапии и повторного оперативного вмешательства может быть предложен тот или иной вид нейромодуляции [1]. На сегодняшний день при ФРЭ наиболее распространены три вида нейромодуляции: стимуляция блуждающего нерва (англ. vagus nerve stimulation, VNS), нейростимуляция с обратной связью (англ. responsive neurostimulation, RNS) и глубокая стимуляция (англ. deep brain stimulation, DBS) переднего ядра таламуса (англ. anterior nucleus of the thalamus, ANT) либо гиппокампа (англ. hippocampus, HP) [4].
Цель – оценка эффективности проведения нейромодуляции у пациентов с ФРЭ после неудачных резекционных хирургических вмешательств.
МАТЕРИАЛ И МЕТОДЫ / MATERIAL AND METHODS
В ретроспективный анализ результатов лечения вошли 23 пациента (12 мужчин и 11 женщин), оперированных по поводу ФРЭ в ФГБУ «Федеральный центр нейрохирургии» Минздрава России (г. Новосибирск) с 2014 по 2022 гг., которым после неудачного оперативного вмешательства проведена имплантация нейромодуляторов с целью VNS-, ANT-DBS- или HP-DBS-терапии. Данные были получены из историй болезни, при очном контрольном посещении пациентами центра в катамнезе, а также при помощи опроса по телефону в случае, если пациент не имел возможности явиться в центр.
Первое оперативное вмешательство / Previous surgery
Всем больным ранее были проведены резекционные вмешательства по поводу ФРЭ, в дальнейшем у них отмечался рецидив приступов. Из 23 пациентов в 4 (17,4%) случаях была проведена левосторонняя медиальная височная лобэктомия (МВЛЭ), в 6 (26,1%) – правосторонняя МВЛЭ, в 3 (13,0%) – селективная амигдалогиппокампэктомия (САГЭ), в 6 (26,1%) – стереотаксическая каллозотомия, в 2 (8,7%) – удаление ганглиоглиомы медиальных отделов височной доли, в 2 (8,7%) – селективное удаление эпилептогенных очагов экстратемпоральной локализации.
Повторная операция в связи с рецидивом приступов после первого хирургического вмешательства выполнена 6 из 23 (26,1%) пациентов. У 1 больного после САГЭ слева проведена переднемедиальная височная лобэктомия, у 1 пациента после удаления ганглиоглиомы медиобазальных отделов правой височной доли с САГЭ справа – правосторонняя МВЛЭ, у 1 пациента после правосторонней МВЛЭ – деструкция эпилептогенных очагов в правой лобной доле, у 1 больного после правосторонней МВЛЭ – имплантация системы VNS, у 2 пациентов после МВЛЭ – расширенная резекция височной доли.
Нейромодуляция / Neuromodulation
Система VNS имплантирована 18 (78,3%) пациентам, система HP-DBS – 3 (13,0%), система ANT-DBS – 2 (8,7%). Одному из пациентов была установлена система VNS, однако в связи с неэффективностью терапии в течение 4 лет она была удалена и имплантирована система HP-DBS.
VNS-терапия
Имплантацию системы VNS проводили под общей анестезией согласно стандартной методике, осуществляли доступ к левому блуждающему нерву по переднему краю грудинно-ключично-сосцевидной мышцы. Затем создавали карман в подкожно-жировой клетчатке для генератора импульсов, электрод проводили подкожно от шеи до кармана. После размещения электрода на блуждающем нерве выполняли его подключение к генератору импульсов и проверку импеданса.
DBS-терапия
Пациенты, которым была имплантирована система DBS, проходили предоперационное обследование, включавшее магнитно-резонансную томографию (МРТ) головного мозга с последовательностями Т1, Т2, FGATIR. Имплантация DBS также проводилась под общей анестезией. После фиксации базового кольца к голове пациента выполнялась мультисрезовая компьютерная томография (МСКТ) головного мозга с базовым кольцом, затем данные МСКТ совмещались с данными МРТ, выполненной накануне, и осуществлялись расчеты стереотаксических траекторий.
Установку электродов проводили передним или задним доступом в зависимости от выбранной мишени (ANT или HP). После имплантации и фиксации электродов выполняли имплантацию удлинителей и генератора импульсов в правую подключичную область. Пациентам в группе HP-DBS проводили одностороннюю стимуляцию контралатерального гиппокампа. Стимуляцию ANT-DBS осуществляли с двух сторон трансвентрикулярным доступом.
Оценка результатов / Assessment of results
Перед имплантацией нейростимулятора результаты хирургии были классифицированы по шкале исходов хирургического лечения эпилепсии Engel [5].
Первичное программирование VNS проводили в среднем через 2 нед после имплантации, а стимулятора глубинных структур – через 1 мес. Результаты VNS-терапии в катамнезе оценивали по шкале McHugh (МН) [6], результаты DBS-терапии – по степени снижения частоты приступов в процентах.
Катамнез составил от 12 до 108 мес (средний катамнез – 56,5 мес).
Этические аспекты / Ethical aspects
Исследование было проведено по принципам Хельсинкской декларации Всемирной медицинской ассоциации (Форталеза, Бразилия, 2013 г.). Все пациенты подписали информированное согласие на участие в исследовании и публикацию материала. Также было получено одобрение этического комитета ФГБУ «Федеральный центр нейрохирургии» Минздрава России (г. Новосибирск) (протокол № 4 от 22 февраля 2023 г.).
Статистический анализ / Statistical analysis
В связи с небольшой когортой пациентов результаты представлены в виде описательной статистики. Данные приведены в числовых значениях с расчетом процентных значений. Для анализа использовалась программа Microsoft Office Excel (Microsoft, США).
РЕЗУЛЬТАТЫ / RESULTS
До установки нейростимулятора исходы вмешательств расценены как Engel 3a у 2 пациентов, Engel 3b – у 2, Engel 4а – у 7, Engel 4b – у 12 (табл. 1).
Таблица 1. Результаты нейромодуляции у пациентов с фармакорезистентной эпилепсией
после неудачных резекционных хирургических вмешательств
Table 1. Outcomes of neuromodulation in patients with drug-resistant epilepsy
after failed resection surgery
Пациент / Patient | Первое оперативное лечение / Previous surgery | Исходный уровень по шкале Engel / Baseline level by Engel scale | Вид нейромодуляции / Neuromodulation type | Исход после имплантации нейростимулятора** / Outcome after neurostimulator implantation** |
1* | Правосторонняя МВЛЭ / Right-sided MTL | Engel 4b | VNS | McHugh V |
2 | Левосторонняя МВЛЭ, расширенная резекция / Left- sided MTL, extended resection | Engel 4a | ANT DBS | >60% |
3 | Правосторонняя МВЛЭ / Right-sided MTL | Engel 4a | ANT DBS | Без изменений / No changes |
4 | Правосторонняя МВЛЭ / Right-sided MTL | Engel 4a | HP DBS | >50% |
5 | Правосторонняя МВЛЭ, расширенная резекция / Right-sided MTL, extended resection | Engel 4b | HP DBS | >50% |
6 | Правосторонняя МВЛЭ / Right-sided MTL | Engel 3b | VNS | McHugh Ia |
7 | Стереотаксическая каллозотомия / Stereotactic callosotomy | Engel 4b | VNS | McHugh IIa |
8 | Стереотаксическая каллозотомия / Stereotactic callosotomy | Engel 4b | VNS | McHugh IIb |
9 | Левосторонняя МВЛЭ / Left-sided MTL | Engel 3a | VNS | McHugh IIIb |
10 | Удаление очага эпилептической активности теменной доли справа / Removed focus of epileptic activity in the right parietal lobe | Engel 4b | VNS | McHugh IIIb |
11 | Стереотаксическая каллозотомия / Stereotactic callosotomy | Engel 4a | VNS | McHugh IIIa |
12 | Левосторонняя МВЛЭ / Left-sided MTL | Engel 4b | VNS | McHugh IIIa |
13 | САГЭ, удаление эпилептогенного очага теменной доли справа / SAH, removed focus of epileptic activity in the right parietal lobe | Engel 4b | VNS | McHugh IIIa |
14 | Левосторонняя МВЛЭ / Left-sided MTL | Engel 4b | VNS | McHugh IIIa |
15 | Правосторонняя САГЭ, правосторонняя МВЛЭ / Right-sided SAH, right- sided MTL | Engel 4b | VNS | McHugh IIIa |
16 | Правосторонняя МВЛЭ, деструкция эпиочагов правой височной доли / Right-sided MTLE, destruction of epifoci in the right temporal lobe | Engel 3a | VNS | McHugh IIIb |
17 | Стереотаксическая каллозотомия / Stereotactic callosotomy | Engel 4a | VNS | McHugh IIIb |
18 | Левосторонняя САГЭ, левосторонняя МВЛЭ / Left-sided SAH, left-sided MTL | Engel 4b | VNS | McHugh IIIb |
19 | Удаление ганглиоглиомы правой лобно-теменной области / Removed ganglioglioma in the right frontoparietal area | Engel 4b | VNS | McHugh IV |
20 | Стереотаксическая каллозотомия / Stereotactic callosotomy | Engel 3b | VNS | McHugh V |
21 | Удаление эпилептогенного образования левой теменной доли / Removed epileptogenic focus in the left parietal lobe | Engel 4a | VNS | McHugh V |
22 | Стереотаксическая каллозотомия / Stereotactic callosotomy | Engel 4a | VNS | McHugh V |
23 | Удаление ганглиоглиомы правой лобной доли / Removed ganglioglioma in the right frontal lobe | Engel 4b | VNS | McHugh V |
Примечание. МВЛЭ – медиальная височная лобэктомия; САГЭ – селективная амигдалогиппокампэктомия; VNS (англ. vagus nerve stimulation) – стимуляция блуждающего нерва; DBS (англ. deep brain stimulation) – глубокая стимуляция мозга; ANT (англ. anterior nucleus of the thalamus) – переднее ядро таламуса; HP (англ. hippocampus) – гиппокамп. * Пациенту 1 в связи с неэффективностью VNS-терапии в течение 4 лет стимулятор был удален и имплантирована система HP-DBS (исход после имплантации второго нейростимулятора – без изменений). ** Исход VNS – по шкале McHugh, исход DBS – снижение частоты приступов (%).
Note. MTL – medial temporal lobectomy; SAH – selective amygdalohippocampectomy; VNS – vagus nerve stimulation; DBS – deep brain stimulation; ANT – anterior nucleus of the thalamus; HP – hippocampus. * Due to ineffective four-year-long VNS therapy in patient 1, the stimulator was removed and HP-DBS system was implanted (related outcome unchanged). ** VNS outcome – by McHugh scale, DBS outcome – reduced seizure rate (%).
VNS-терапия / VNS therapy
В группе пациентов с имплантированной системой VNS исход терапии составил MH Ia–IIIb в 13 случаях (72,2%), из них исход MH Ia–IIb отмечен у 3 (16,7%) больных, MH IIIa–IIIb – у 10 (55,5%). Исход MH IV–V зарегистрирован у 5 (27,8%) пациентов (рис. 1).
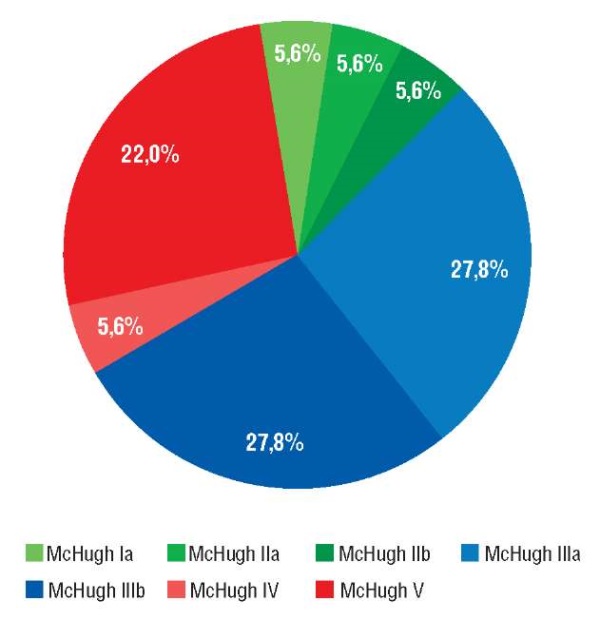
Рисунок 1. Исходы после имплантации системы стимуляции блуждающего нерва
(англ. vagus nerve stimulation, VNS) по шкале McHugh
Figure 1. Outcomes after vagus nerve stimulator (VNS) implantation by McHugh scale
DBS-терапия / DBS therapy
В группе HP-DBS у 2 пациентов отмечено снижение частоты приступов более чем на 50% от исходного уровня в течение 2 лет наблюдения (см. табл. 1). У 1 больного снижения частоты приступов не зарегистрировано, однако наблюдалось некоторое облегчение их тяжести, при этом противосудорожная терапия не менялась.
В группе ANT-DBS у одного пациента отмечено снижение частоты приступов на 60% и облегчение тяжести приступов, у второго изменений в частоте приступов не наблюдалось.
ОБСУЖДЕНИЕ / DISCUSSION
На сегодняшний день при ФРЭ наиболее распространены три вида нейромодуляции: VNS, RNS, ANT-DBS и HP-DBS.
Предполагается, что механизм действия VNS основан на нейромодуляции ствола головного мозга, таламических и кортикальных афферентных проекций, включая катехоламинергические ядра и лимбические участки. Долгосрочный эффект снижения частоты приступов при VNS-терапии может быть обусловлен и другими механизмами, такими как модуляция ГАМК-ергической1 функции. Механизм ANT-DBS при эпилепсии все еще не до конца изучен. Хроническая стимуляция переднего ядра таламуса усиливает ГАМК-ергическую нейротрансмиссию и уменьшает интериктальную активность гиппокампа у лиц с мезиальной височной эпилепсией. Система RNS предназначена для непрерывного мониторинга внутричерепной электроэнцефалографической картины в зоне или зонах начала приступа и проведения кратковременной высокочастотной стимуляции при обнаружении иктальных паттернов для предотвращения эпиприступа [4].
В настоящее время существует достаточное количество исследований, посвященных эффективности нейромодуляции у пациентов после неудачных хирургических операций.
Так, A.P. Amar et al. (2008 г.) [7] на основе данных VNS Therapy Patient Outcome Registry (США) сравнили группы пациентов, которым была имплантирована VNS-система, при этом больные 1-й группы (n=921) до имплантации перенесли хирургическое лечение, а пациентам 2-й группы (n=3822) оперативное вмешательство не проводилось. Средняя величина снижения частоты приступов в 1-й группе составила 42,5% через 3 мес наблюдения с последующим увеличением этого показателя до 50,5% через 24 мес, при этом количество пациентов, ответивших на терапию, достигло 55%. Во 2-й группе средняя величина снижения приступов составила 47,0% через 3 мес наблюдения и 66,7% через 24 мес, а количество пациентов, ответивших на терапию, – 62%. Анализ качества жизни этих больных показал тенденцию к его улучшению с течением времени. Тем не менее авторы отмечают, что сведения, полученные из национального реестра, могут быть недостоверными в связи с систематической ошибкой в отчетности и отборе пациентов [7].
F.L. Vale et al. (2011 г.) [4] приводят данные 37 пациентов с ФРЭ и неудовлетворительными результатами резекционного лечения (лобэктомия или каллозотомия), которым была имплантирована система VNS. Уровень снижения частоты приступов составил менее 30% у 24 (64,9%) больных, 30–60% – у 9 (24,3%) и более 60% – у 4 (10,8%) пациентов.
В 2010 г. опубликованы результаты SANTÉ trial (англ. Stimulation of Anterior Nucleus of Thalamus for Epilepsy) [1] – мультицентрового рандомизированного контролируемого исследования, включившего 110 пациентов с фокальной ФРЭ. Всем больным была имплантирована система ANT-DBS. Через 3 мес слепой фазы исследования частота приступов снизилась в среднем на 40% в группе стимуляции и на 15% в контрольной группе (в сравнении с дооперационным периодом). Но наряду с этим в группе стимуляции чаще отмечались субъективная депрессия и снижение памяти. Интересно, что в обеих группах в течение 1-го месяца после имплантации и до начала стимуляции наблюдалось снижение частоты приступов примерно на 22%, что говорит о наличии «повреждающего эффекта» – немедленного уменьшения частоты приступов, вызванного повреждением нервной ткани в результате имплантации электрода. Затем всем пациентам проводилась нейростимуляция, на фоне которой отмечено прогрессирующее снижение частоты приступов в среднем на 69% в течение 5 лет наблюдения. У 68% больных частота приступов снизилась наполовину, а также зарегистрировано существенное уменьшение их тяжести и улучшение качества жизни. Анализ подгрупп показал, что лучшие результаты имели пациенты с височной эпилепсией (при стимуляции во время слепой фазы исследования среднее снижение частоты приступов в этой группе составило 44,2% при 40% для всей группы больных, получавших стимуляцию). Точно так же через 5 лет в группе пациентов с височной эпилепсией среднее снижение частоты приступов составило 76% по сравнению с 59% в группе больных лобной эпилепсией и 68% у пациентов с другими формами эпилепсии. В связи с недавним закрытием исследования были опубликованы результаты 10-летнего катамнеза пациентов. Через 10 лет активными участниками оставались 57 человек из 110, медиана снижения частоты приступов составила 75% вне зависимости от того, проводилась ранее VNS или резекционная хирургия. Снижение частоты билатеральных тонико-клонических приступов составило 71%. Добавление новых противоэпилептических препаратов не повлияло на частоту приступов [1].
P. Ding et al. (2016 г.) [8] приводят данные по результатам односторонней стимуляции гиппокампа у 5 пациентов с битемпоральной ФРЭ после неудачной передне-медиальной височной лобэктомии. В этом исследовании 18 больным битемпоральной эпилепсией выполнена передне-медиальная височная лобэктомия (операция проводилась на стороне, с которой было зарегистрировано не менее 2/3 приступов). При этом количество пациентов без приступов после хирургического вмешательства составило 55,6% (10/18) через 1 год, 50,0% (9/18) через 2 года и 44,4% (4/9) через 5 лет. Результаты хирургического лечения оказались значительно лучше, чем в контрольной группе, состоявшей из 12 больных, которым проводилась медикаментозная терапия. Затем 5 пациентам была выполнена имплантация системы НР-DBS в гиппокамп, контралатеральный стороне операции. На фоне DBS-терапии отмечено снижение частоты приступов на 80–100%, а также 80% больных избавились от приступов через 1 год наблюдения [8].
Существует ряд исследований, посвященных сравнению эффективности различных методик нейромодуляции у пациентов с ФРЭ. J. Zhu et al. (2021 г.) [10] описывают лучшую эффективность после ANT-DBS в сравнении с VNS в серии у 35 пациентов. Другие авторы (V. Shah et al. (2019 г.) [10], T. Kulji et al. (2017 г.) [11], J.D. Rolston et al. (2012 г.) [12]) не указывают на преобладание эффективности какого-либо метода нейромодуляции. Выбор метода основывается на индивидуальных клинических особенностях больного, таких как возраст на момент вмешательства, длительность заболевания, тип приступов и количество резективных операций по поводу эпилепсии в анамнезе, а также на предпочтениях конкретного пациента [9–12].
В нашем исследовании как VNS-, так и DBS-терапия показали неплохую эффективность в снижении частоты приступов у пациентов с ФРЭ, однако следует учитывать достаточно малое количество больных в группе DBS-терапии, а также использование различных мишеней. Необходимо отметить, что часть пациентов в группе VNS-терапии проходила последующую настройку нейростимуляции у эпилептолога по месту жительства, а не в нашем центре.
ЗАКЛЮЧЕНИЕ / CONCLUSION
Нейромодуляция позволяет значимо уменьшить частоту приступов и улучшить качество жизни у более чем половины пациентов с ФРЭ после неудачного оперативного лечения. По результатам нашего исследования, эффективность нейростимуляции наблюдалась более чем в 50% случаев. Для сравнения эффективности различных видов нейромодуляции необходимо проведение дальнейших исследований с большей выборкой пациентов.
1. ГАМК – гамма-аминомасляная кислота.
Список литературы
1. Salanova V., Sperling M.R., Gross R.E., et al. The SANTÉ study at 10 years of follow-up: effectiveness, safety, and sudden unexpected death in epilepsy. Epilepsia. 2021; 62 (6): 1306–17. https://doi.org/10.1111/epi.16895.
2. Эпилепсия. Доклад Генерального директора Всемирной организации здравоохранения. 146-я сессия EB146/12, 25 ноября 2019 г. URL: https://apps.who.int/gb/ebwha/pdf_files/EB146/B146_12-ru.pdf (дата обращения 20.02.2024).
3. Ryvlin P., Rheims S., Hirsch L.J., et al. Neuromodulation in epilepsy: state-of-the-art approved therapies. Lancet Neurol. 2021; 20 (12): 1038–47. https://doi.org/10.1016/S1474-4422(21)00300-8.
4. Vale F.L., Ahmadian A., Youssef A.S., et al. Long-term outcome of vagus nerve stimulation therapy after failed epilepsy surgery. Seizure. 2011; 20 (3): 244–8. https://doi.org/10.1016/j.seizure.2010.12.003.
5. Engel J.V.N.P. Jr., Rasmussen T.B., Ojemann L.M. (Eds.) Outcome with respect to epileptic seizures. New York: Raven Press; 1993: 609–21.
6. McHugh J.C., Singh H.W., Phillips J., et al. Outcome measurement after vagal nerve stimulation therapy: proposal of a new classification. Epilepsia. 2007; 48 (2): 375–8. https://doi.org/10.1111/j.1528-1167.2006.00931.x.
7. Amar A.P., Apuzzo M.L., Liu C.Y. Vagus nerve stimulation therapy after failed cranial surgery for intractable epilepsy: results from the vagus nerve stimulation therapy patient outcome registry. Neurosurgery. 2004; 55 (5): 1086–93. https://doi.org/10.1227/01.neu.0000141073.08427.76.
8. Ding P., Zhang S., Zhang J., et al. Contralateral hippocampal stimulation for failed unilateral anterior temporal lobectomy in patients with bilateral temporal lobe epilepsy. Stereotact Funct Neurosurg. 2016; 94 (5): 327–35. https://doi.org/10.1159/000449008.
9. Zhu J., Wang X., Xu C., et al. Comparison of efficiency between VNS and ANT-DBS therapy in drug-resistant epilepsy: a one year follow up study. J Clin Neurosci. 2021; 90: 112–7. https://doi.org/10.1016/j.jocn.2021.05.046.
10. Shah V., Eliashiv D., Reider-Demer M. Neurostimulation & Epilepsy. For medically refractory epilepsy, neurostimulation options – old and new – provide new hope. URL: https://practicalneurology.com/articles/2019-oct/neurostimulation-epilepsy/pdf (дата обращения 20.02.2024).
11. Kulju T., Haapasalo J., Lehtimäki K., et al. Similarities between the responses to ANT-DBS and prior VNS in refractory epilepsy. Brain Behav. 2018; 8 (6): e00983. https://doi.org/10.1002/brb3.983.
12. Rolston J.D., Englot D.J., Wang D.D., et al. Comparison of seizure control outcomes and the safety of vagus nerve, thalamic deep brain, and responsive neurostimulation: evidence from randomized controlled trials. Neurosurg Focus. 2012; 32 (3): E14. https://doi.org/10.3171/2012.1.FOCUS11335.
Об авторах
Ф. А. ЕфремовРоссия
Ефремов Федор Алексеевич – врач-нейрохирург отделения функциональной нейрохирургии.
ул. Немировича-Данченко, д. 132/1, Новосибирск 630087
Р. В. Агаев
Россия
Агаев Расим Вугар оглы – врач-нейрохирург отделения функциональной нейрохирургии.
ул. Немировича-Данченко, д. 132/1, Новосибирск 630087
С. А. Ким
Россия
Ким Сергей Афанасьевич – врач-нейрохирург отделения функциональной нейрохирургии.
ул. Немировича-Данченко, д. 132/1, Новосибирск 630087
Г. И. Мойсак
Россия
Мойсак Галина Ивановна – к.м.н., врач-невролог отделения функциональной нейрохирургии.
ул. Немировича-Данченко, д. 132/1, Новосибирск 630087
Scopus Author ID 57088972500
Е. Д. Анисимов
Россия
Анисимов Егор Дмитриевич – врач-нейрохирург отделения функциональной нейрохирургии.
ул. Немировича-Данченко, д. 132/1, Новосибирск 630087
Е. А. Хабарова
Россия
Хабарова Елена Александровна – врач-невролог отделения функциональной нейрохирургии.
ул. Немировича-Данченко, д. 132/1, Новосибирск 630087
Д. А. Рзаев
Россия
Рзаев Джамиль Афетович – к.м.н., главный врач ФГБУ «ФЦН» Минздрава России; доцент кафедры нейронаук Института медицины и психологии ФГБОУ ВО «НГМУ» Минздрава России.
ул. Немировича-Данченко, д. 132/1, Новосибирск 630087; Красный пр-т, д. 52, Новосибирск 630091
Рецензия
Для цитирования:
Ефремов Ф.А., Агаев Р.В., Ким С.А., Мойсак Г.И., Анисимов Е.Д., Хабарова Е.А., Рзаев Д.А. Оценка эффективности нейромодуляции у пациентов с фармакорезистентной эпилепсией после неудачного хирургического лечения. Эпилепсия и пароксизмальные состояния. 2024;16(2):96-103. https://doi.org/10.17749/2077-8333/epi.par.con.2024.184
For citation:
Efremov F.A., Agaev R.V., Kim S.A., Moisak G.I., Anisimov E.D., Khabarova E.A., Rzaev J.A. Effectiveness of neuromodulation in patients with drug-resistant epilepsy after failed surgical treatment. Epilepsy and paroxysmal conditions. 2024;16(2):96-103. https://doi.org/10.17749/2077-8333/epi.par.con.2024.184
JATS XML

Контент доступен под лицензией Creative Commons Attribution-NonCommercial-ShareAlike 4.0 International License.







































