Перейти к:
Обзор методов математического анализа ЭЭГ. Количественная ЭЭГ
https://doi.org/10.17749/2077-8333/epi.par.con.2023.154
Аннотация
Целью данной статьи является знакомство медицинских специалистов, занимающихся регистрацией и анализом электроэнцефалографических (ЭЭГ) исследований, с методами математической обработки и компьютерного анализа записанных ЭЭГ-данных. Понимание принципов работы инструментов количественного анализа ЭЭГ должно помочь медицинскому персоналу правильно использовать их возможности и в конечном итоге повысить качество медицинского обслуживания. В статье рассмотрены базовые и инновационные математические инструменты для обработки и анализа ЭЭГ.
Ключевые слова
Для цитирования:
Иванов А.А. Обзор методов математического анализа ЭЭГ. Количественная ЭЭГ. Эпилепсия и пароксизмальные состояния. 2023;15(2):171–192. https://doi.org/10.17749/2077-8333/epi.par.con.2023.154
For citation:
Ivanov А.А. Overview of mathematical EEG analysis. Quantitative EEG. Epilepsy and paroxysmal conditions. 2023;15(2):171–192. (In Russ.) https://doi.org/10.17749/2077-8333/epi.par.con.2023.154
ВВЕДЕНИЕ / INTRODUCTION
Современный цифровой комплекс для регистрации электроэнцефалографических (ЭЭГ) сигналов является сложным с технической точки зрения оборудованием [1][2]. Компьютерные системы для регистрации и анализа ЭЭГ содержат большой набор математических методов обработки и анализа сигнала ЭЭГ. Разобраться в них бывает совсем непросто, а использовать на практике без понимания принципов их работы – невозможно.
В первых двух статьях этого цикла мы уже подробно описывали устройство компьютерного энцефалографа [2] и возможности современного программного обеспечения (ПО) [3]. Теперь же сконцентрируемся на методах математической обработки ЭЭГ и их применимости в клинической практике. В данной статье рассмотрены как базовые, так и инновационные инструменты компьютерной обработки ЭЭГ-сигналов, знакомство с которыми позволит специалистам более детально и точно оценивать ЭЭГ.
Материал содержит описание математических методов анализа ЭЭГ на примере программы «Нейрон-Спектр.NET» (ООО «Нейрософт», Россия). Однако он будет полезен и специалистам, работающим на любом другом современном ЭЭГ-комплексе, т.к. возможности ПО в них схожи.
КОЛИЧЕСТВЕННАЯ ЭЭГ / QUANTITATIVE EEG
Начиная с 1990-х гг. с развитием компьютерной техники постоянно появляются различные методы компьютерной обработки и анализа ЭЭГ-сигналов. Многие из них в настоящее время широко применяются, другие являются более экзотическими и используются только в научных исследованиях. Цифровое представление ЭЭГ в том или ином виде стали называть количественной ЭЭГ. В отличие от визуальной оценки ЭЭГ, количественное ее представление позволяет объективизировать результаты оценки, сравнить различные эпизоды записи между собой, оценить динамику изменения ЭЭГ во времени.
Цифровая фильтрация / Digital filtering
Прежде всего для качественной обработки данных ЭЭГ сигнал необходимо отфильтровать в заданной полосе частот. В соответствии с Рекомендациями экспертного совета по нейрофизиологии Российской противоэпилептической лиги (РПЭЛ) по проведению рутинной ЭЭГ [4] сигнал ЭЭГ должен быть отфильтрован в полосе от 0,5 до 70 Гц [5–7]. Именно в этой полосе частот лежит основной полезный сигнал. Для фильтрации применяются цифровые фильтры [8].
Фильтр верхних частот (ФВЧ)
ФВЧ помогает отфильтровать паразитные медленноволновые колебания, справиться с постоянной составляющей на ЭЭГ. Иногда для анализа сверхмедленной ЭЭГ-активности данный фильтр отключают или устанавливают значения, близкие к 0 Гц. Диапазон установки ФВЧ – от 0,01 до 10 Гц.
Фильтр нижних частот (ФНЧ)
ФНЧ помогает отфильтровать быстрые частоты, которые не нужно видеть на ЭЭГ (например, миографический артефакт). Раньше этот фильтр традиционно устанавливался в значение 35 Гц, но в современных рекомендациях [4–7][9] прописано значение 70 Гц. Это связано с тем, что ФНЧ на 35 Гц может существенно снижать амплитуду спайков и острых волн, частота которых превышает 35 Гц. При желании просмотреть и проанализировать более высокие частоты этот фильтр можно отключить или установить более высокие значения частоты среза. Диапазон установки ФНЧ – от 15 до 500 Гц.
Режекторный фильтр
Режекторный фильтр предназначен для подавления синфазной помехи от питающей сети (50 или 60 Гц в зависимости от региона). Обычно в качестве режекторного применяется рекурсивный фильтр, но его недостаток состоит в том, что он вырезает частоты около 50 Гц из сигнала, и если в этой частотной области будет находиться полезный сигнал (например, спайки и острые волны), то он тоже подвергнется резекции. В современных компьютерных программах помимо рекурсивного применяется так называемый адаптивный режекторный фильтр, который вырезает из сигнала только чистую синусоиду 50 Гц, не повреждая полезный сигнал.
Полосовой фильтр
Полосовые фильтры могут применяться для того, чтобы дополнительно отфильтровать сигнал в заданной полосе частот. Например, с помощью такого фильтра можно отфильтровать только альфа-диапазон от 8 до 14 Гц.
Современное ПО позволяет хранить в обследовании так называемые сырые, т.е. нефильтрованные данные. Фильтрация в этом случае проводится «на лету», непосредственно во время просмотра ЭЭГ-сигнала на экране компьютера. Подобный подход позволяет в любой момент переключить фильтры или полностью их отключить. Следует помнить, что от правильной установки частот фильтров зависит форма ЭЭГ-сигнала и его дальнейшая интерпретация [8][9].
Эпохи анализа / Epochs of analysis
Запись ЭЭГ-обследования обычно довольно сложно провести без различных артефактов. Обычно артефакты исключаются из обсчета и анализа. Для анализа ЭЭГ-сигнала предварительно отбираются стабильные участки записи – так называемые эпохи анализа. В современных программах обработки и анализа ЭЭГ применяется два типа анализа:
- экспресс-анализ предназначен для быстрого анализа без необходимости выделения эпох (как правило, применяется при онлайн-анализе во время регистрации ЭЭГ, при анализе видимой на экране части ЭЭГ-кривых или выделенного фрагмента ЭЭГ);
- анализ эпох требует предварительного их выделения (результаты анализа всех эпох усредняются либо по всей записи, либо отдельно по функциональным пробам) [3].
Длительность эпохи анализа по умолчанию обычно составляет 5 с, но может быть задана индивидуально. Выделение эпох анализа может осуществляться как вручную, так и в автоматическом режиме.
После того как все безартефактные участки записи размечены как эпохи, можно приступать к их математической обработке.
Часто применяемые виды количественного анализа ЭЭГ-сигналов / Commonly used types of EEG signals quantitative analysis
Амплитудный анализ
Это один из первых и наиболее понятных и распространенных видов математического анализа ЭЭГ [10–13]. Раньше, в эпоху докомпьютерной ЭЭГ, чтобы точно измерить амплитуду волн ЭЭГ, кривые распечатывали на миллиметровой бумаге. Теперь все расчеты выполняет компьютер.
Существует два варианта измерения амплитуды ЭЭГ-сигнала: «пик – пик» и «изолиния – пик». В настоящее время применяется в основном первый вариант – измерение амплитуды от пика до пика. Измерение амплитуды волн от изолинии сопряжено с проблемой постоянной составляющей на ЭЭГ, которая может сдвигать сигнал относительно изолинии.
В процессе вычисления амплитуд компьютерная программа разделяет каждую ЭЭГ-кривую на отдельные волны. Кроме измерения амплитуды каждой волны также можно измерить и ее длительность, т.е. период. Зная период волны, можно рассчитать ее частоту как величину, обратную периоду. Таким образом, результаты расчета амплитуд ЭЭГ-сигнала могут быть разделены по ритмам волн (дельта, тета, альфа, бета) и представлены в виде табличной информации, диаграмм или топографических карт. Существует несколько инструментов для амплитудного анализа. Например, можно просто просмотреть абсолютные числовые значения по каждой кривой ЭЭГ в любой момент времени (рис. 1а). В специальном режиме измерения волны компьютерная программа может рассчитать амплитудные параметры выделенного участка кривой (рис. 1b).

Рисунок 1. Измерение мгновенных амплитуд по всем записанным ЭЭГ-кривым:
a – абсолютные значения амплитуд относительно изолинии выводятся слева от названия отведений и представлены в виде топографической карты, с помощью которой можно наглядно оценить пространственное распределение электрической активности по скальпу в момент времени, отмеченный вертикальным маркером красного цвета (перемещая маркер с помощью мыши, можно оценить изменение ЭЭГ-активности на топографической карте); b – режим измерения волны позволяет рассчитать не только амплитуду выделенной волны, но и среднюю, максимальную амплитуду волн, их доминирующую и среднюю частоту в выделенном участке кривой, отмеченном желтым цветом (фоновая подсветка выбранной кривой имеет размах 50 мкВ и позволяет оценить абсолютные амплитуды волн)
Figure 1. Assessing instantaneous amplitudes for all recorded EEG curves:
a – absolute values of amplitudes relative to the isoline are depicted to the left of the names of the leads and presented as a topographic map to visualize spatial distribution of electrical activity over the scalp at the time point denoted with a red vertical marker (by moving the marker with the mouse, it allows to evaluate change in EEG activity on topographic map); b – wave measurement mode allows to calculate not only the selected wave amplitude, but also average and maximum amplitudes, dominant and average frequency of waves in the selected curve section highlighted in yellow (the background illumination of selected curve has a range of 50 μV to evaluate wave absolute amplitudes)
Вообще само по себе абсолютное значение амплитуды ЭЭГ не несет сколь-нибудь значимой диагностической информации. Высокая или низкая амплитуда ЭЭГ может быть индивидуальной особенностью каждого конкретного человека. Амплитудных норм ЭЭГ не существует. Однако, например, оценка изменения амплитуды ЭЭГ, измерение ее динамики в зависимости от состояния пациента – это уже значимые в диагностическом плане параметры. И с помощью амплитудного анализа такая оценка становится легко реализуемой.
Для отслеживания изменения амплитуды ЭЭГ во времени начиная от заданного момента используется так называемая амплитудная развертка, которая формирует амплитудные срезы с заданным временным интервалом (рис. 2).
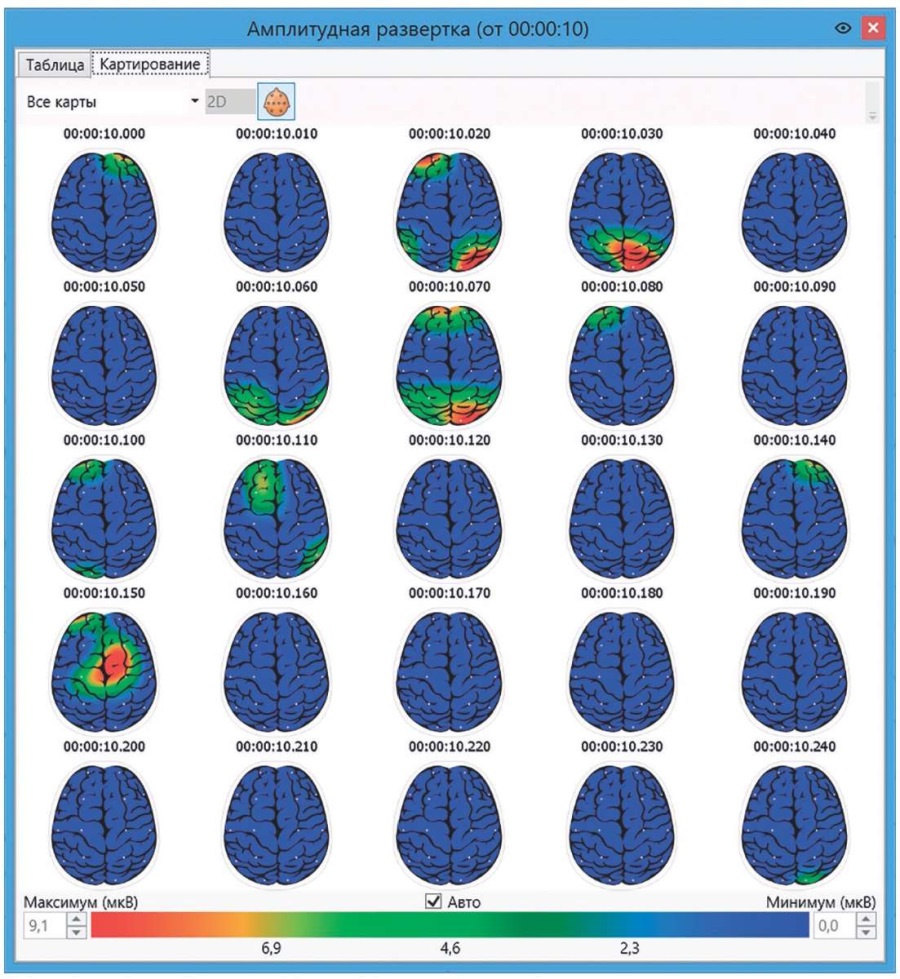
Рисунок 2. Амплитудная развертка
Figure 2. Amplitude sweep
Чтобы рассчитать средние, максимальные амплитуды ритмов волн, межполушарную асимметрию по амплитуде, используется специальное окно амплитудного анализа. В нем можно выбрать параметр для анализа (средняя, максимальная амплитуда, асимметрия и др.) и выводить его в виде таблицы значений по каждому отведению (рис. 3а). В расчет принимается либо выделенный участок ЭЭГ-кривых (экспресс-анализ), либо выделенные эпохи анализа (анализ эпох). Наглядно представить табличные данные можно с помощью диаграмм (рис. 3b), а также топографических карт, которые позволяют оценить распределение амплитуд электрической активности по скальпу (рис. 3c).
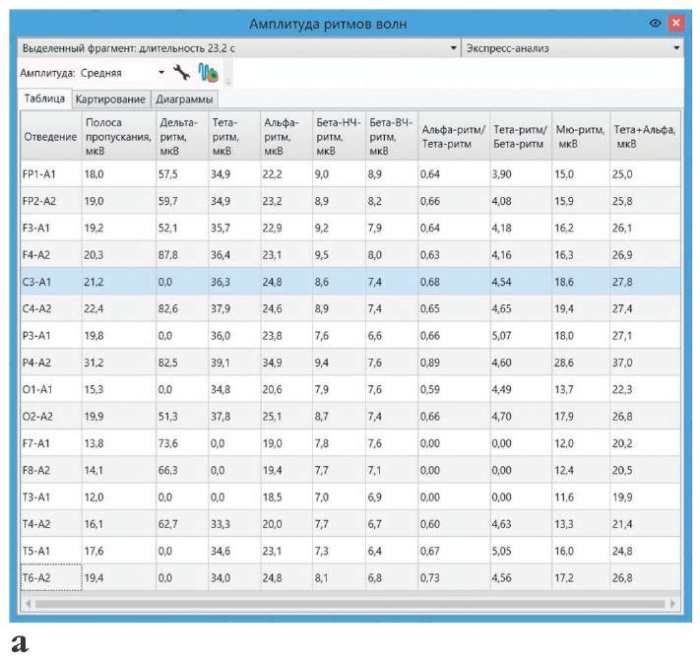
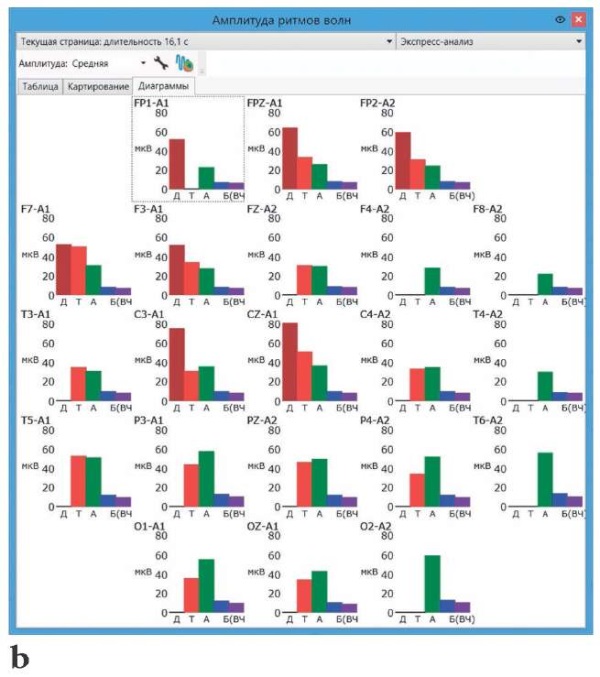
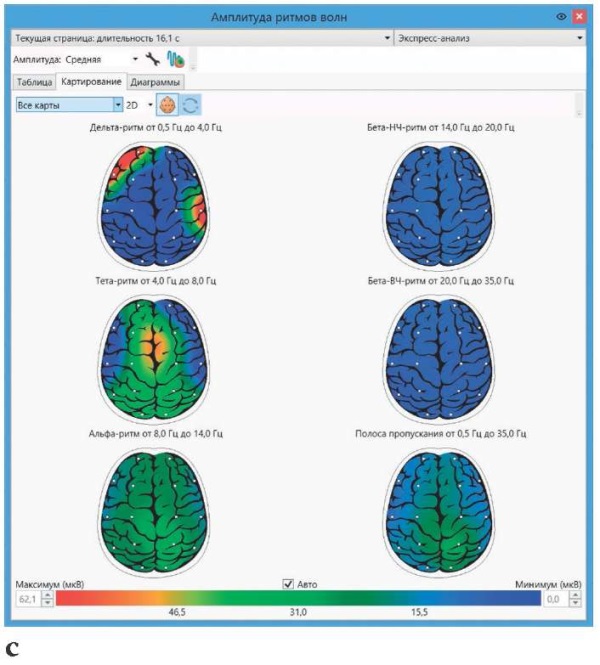
Рисунок 3. Пример расчета средних амплитуд ЭЭГ по ритмам волн:
a – таблица отображает среднюю амплитуду каждого ритма волн для каждого отведения;
b – диаграммы более наглядно представляют ту же информацию, которая была выведена в таблице (например, на диаграмме сразу видно, что во фронтальных отведениях доминирует дельта-ритм, а в затылочных отведениях средняя амплитуда альфа-ритма превалирует над другими ритмами);
с – топографическое картирование с помощью цветовой шкалы отображает распределение амплитуды электрической активности по скальпу
Figure 3. Representative wave rhythm-based calculation of average EEG amplitudes:
a – average amplitude of each wave rhythm paired lead is shown in Table;
b – the diagrams more clearly represent the same data shown in Table (e.g., the diagram immediately shows that the delta rhythm dominates in the frontal leads, whereas in the occipital leads an average amplitude of the alpha rhythm prevails over other rhythms);
c – topographic mapping using a color scale displays amplitude distribution for electrical activity over the scalp
Спектральный анализ
Вторым по частоте использования при анализе ЭЭГ является спектральный анализ. С помощью преобразования Фурье сигнал ЭЭГ переводится из временной в частотную область [13]. На графиках мощности спектра можно видеть, какие частоты доминируют в сигнале (рис. 4).

Рисунок 4. Графики мощности спектра строятся по результатам преобразования Фурье. На данном примере отчетливо видно доминирование дельта-ритма (0,5–4 Гц) в лобных отведениях (возможно, артефакт окулограммы) и альфа-ритма (8–14 Гц) – в затылочных отведениях. Низкочастотный (НЧ) бета-ритм (14–20 Гц) и высокочастотный (ВЧ) бета-ритм (20–35 Гц) практически не представлены в анализируемом участке записи. С помощью маркера можно выбрать конкретную частоту для топографического картирования ее мощности
Figure 4. Representative spectrum power plots are created based on Fourier transform data. The dominance of delta rhythm (0.5–4 Hz) in the frontal leads (likely an oculogram artifact) and alpha rhythm (8–14 Hz) in the occipital leads. Virtually no low-frequency beta rhythm (14–20 Hz) and high-frequency beta rhythm (20–35 Hz) are observed in the section analyzed. Using the marker, it allows to select a specific frequency for power-based topographic mapping
В отличие от амплитуды ЭЭГ, спектральный состав электрической активности можно нормировать в зависимости от состояния пациента. Например, известно, что во сне у человека доминируют низкочастотные волны тета- и дельта-диапазонов, а в состоянии спокойного бодрствования – альфа-волны, наиболее выраженные в окципитальных отведениях [10][11]. Спектральный анализ позволяет визуально оценить распространение тех или иных частот ЭЭГ по скальпу.
Кроме графиков в окнах спектрального анализа также можно использовать табличные результаты анализа, в которых по графикам мощности (в т.ч. и по ритмам волн) вычисляются следующие параметры:
- максимальная мощность рассчитывается как пик графика спектра в заданном частотном диапазоне;
- средняя мощность – усредненная мощность спектра в заданном частотном диапазоне;
- полная мощность – площадь под графиком спектра в заданном частотном диапазоне;
- индекс ритма – отношение площади под графиком спектра в частотном диапазоне ритма к общей площади под графиком спектра в полосе пропускания;
- доминирующая частота – частота, в которой график спектра достигает пика в заданном частотном диапазоне;
- средняя частота – частота, разбивающая площадь под графиком спектра в заданном частотном диапазоне на две равные по площади половины;
- межполушарная асимметрия – разница средней мощности спектра между соответствующими отведениями левого и правого полушарий.
Каждый из этих расчетных параметров можно вывести на топографические карты (рис. 5).
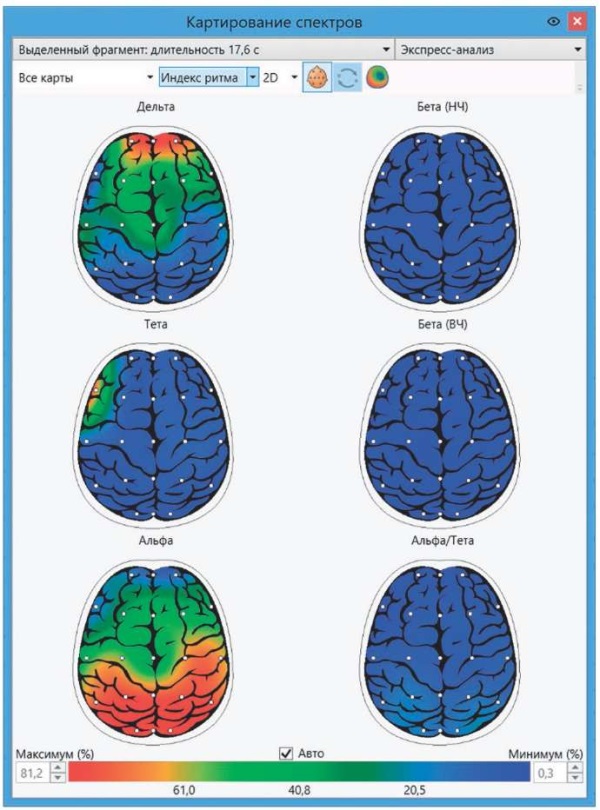
Рисунок 5. Топографические карты индекса ритма по спектру. В данном примере отчетливо видно доминирование альфа-ритма в затылочных отведениях. Красный цвет на картах соответствует максимальному индексу 81,2%, синий – минимальному 0,3%. Зеленый цвет соответствует индексу 40,8%
Figure 5. Topographically mapped spectrum-based rhythm index. The dominance of alpha rhythm in the occipital leads is clearly observed. On the maps, red and blue colors denote the maximum and minimum index comprising 81.2% and 0.3%, respectively. Green color denotes the index of 40.8%
Топографическое картирование
Рассмотрим подробнее инструмент топографического картирования [3]. Чтобы эффективно им пользоваться, необходимо четко представлять, как он работает и какие данные мы видим на карте.
Для примера возьмем топографическую карту полной мощности спектра для альфа-ритма. В первую очередь для построения карты необходимо рассчитать полную мощность спектра в альфа-диапазоне по каждому отведению. Затем, зная расположение электродов на голове (по международной системе «10–20%» [14][15]), можно методом интерполяции рассчитать значения мощности альфа-диапазона в каждой точке на скальпе. После этого, применив палитру цветов, в которой каждому значению мощности соответствует определенный цвет, можно построить цветную карту мощности.
Пример топографической карты мощности альфа-ритма с выведенными значениями под каждым электродом приведен на рисунке 6а. Цветовая палитра может быть задана произвольно по усмотрению пользователя, например как на рисунке 6b. Полученную топографическую карту можно представить как в двумерном, так и в трехмерном виде (рис. 7).

Рисунок 6. Примеры топографического картирования мощности спектра альфа-ритма:
a – под топографической картой представлена текущая цветовая палитра, максимальная мощность (86 мкВ2) обозначена красным, минимальная (7 мкВ2) – синим, средняя – зеленым цветом (в затылочных отведениях мощность спектра альфа-ритма максимальна и составляет 86,5 мкВ2); b – та же самая топографическая карта индекса альфа-ритма в сине-белой палитре (четко видно, что индекс альфа-ритма достигает максимальных значений (до 81,2%) в затылочных отведениях)
Figure 6. Representative topographic mapping of alpha rhythm spectrum power:
a – the current color palette is shown under the topographic map, the maximum (86 µV2), minimum (7 µV2) and average (in the occipital leads, the power of alpha rhythm spectrum is maximum and amounts to 86.5 µV2) power is highlighted in red, blue, and green, respectively; b – similar topographic map of the alpha rhythm index is depicted in blue and white palette (the alpha rhythm index clearly observed to reach its maximum magnitude (up to 81.2%) in the occipital leads)
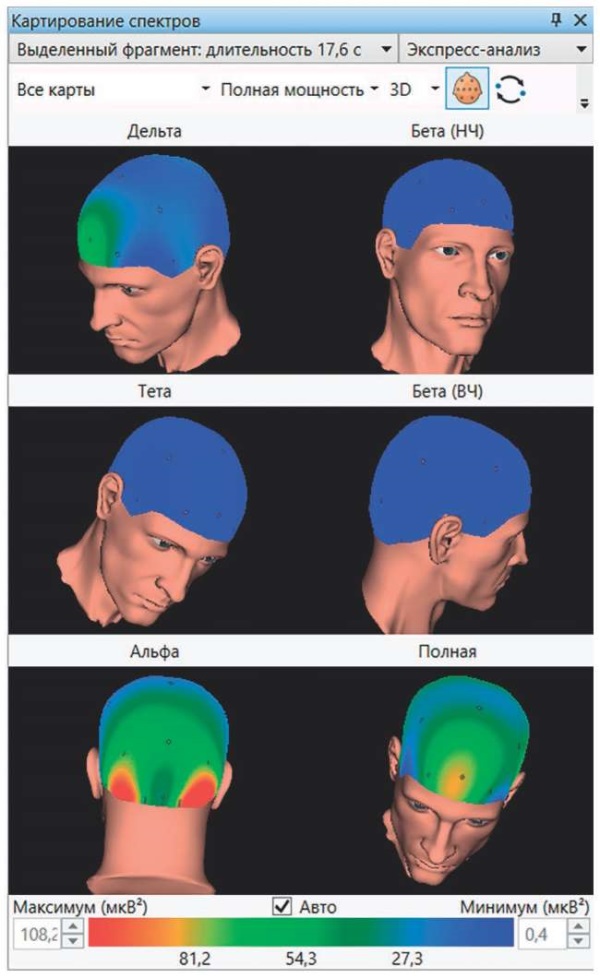
Рисунок 7. 3D-картирование полной мощности спектров ЭЭГ по ритмам
Figure 7. 3D mapping of rhythm-based full power EEG spectra
Корреляционный анализ
В тех случаях, когда требуется оценить сходство ЭЭГ-активности в различных участках головного мозга, поможет корреляционный анализ [12][13][16]. Существует две основные формы корреляционного анализа ЭЭГ:
- автокорреляционный анализ позволяет выяснить степень соответствия сигнала ЭЭГ самому себе с течением времени (применяется расчет автокорреляционной функции сигнала с заданным сдвигом по времени);
- кросскорреляционный анализ показывает соответствие сигналов двух разных отведений друг другу (рис. 8).
В норме ЭЭГ-активность здорового человека должна быть гармонизирована и в некоторой степени единообразна. Если есть структуры, генерирующие резко отличающийся по форме сигнал, они могут быть патологическими.
Выбирая пары ЭЭГ-отведений для расчета функции кросскорреляции, можно обнаружить область головного мозга, активность которой слабо связана с остальными. Топографические карты в данном случае представляют собой набор линий, связывающих выбранные отведения. Цвет линии отображает степень их корреляции и задается выбранной цветовой шкалой.

Рисунок 8. Примеры функции кросскорреляции:
а – функция рассчитана от лобных к затылочным отведениям (чем выше амплитуда колебаний кросскорреляционной функции, тем выше подобие ЭЭГ-активности в этой паре отведений);
b – функция рассчитана от левых к правым отведениям
Figure 8. Representative cross-correlation function:
а – the function was calculated from the frontal to occipital leads (the higher the amplitude of fluctuations for cross-correlation function, the higher similarity of EEG activity in this pair of leads);
b – the function was calculated from the left to the right leads
Когерентный анализ
Этот вид анализа очень похож на корреляционный с тем лишь отличием, что здесь сравнивается не форма исходного ЭЭГ-сигнала, а рассчитанные графики спектров по каждому отведению (рис. 9) [12][13].
Сравнивая между собой частотный состав разных отведений, можно определить области головного мозга, работающие несинхронно с остальными. Низкий уровень когерентности свидетельствует о слабой связности разных структур головного мозга между собой.
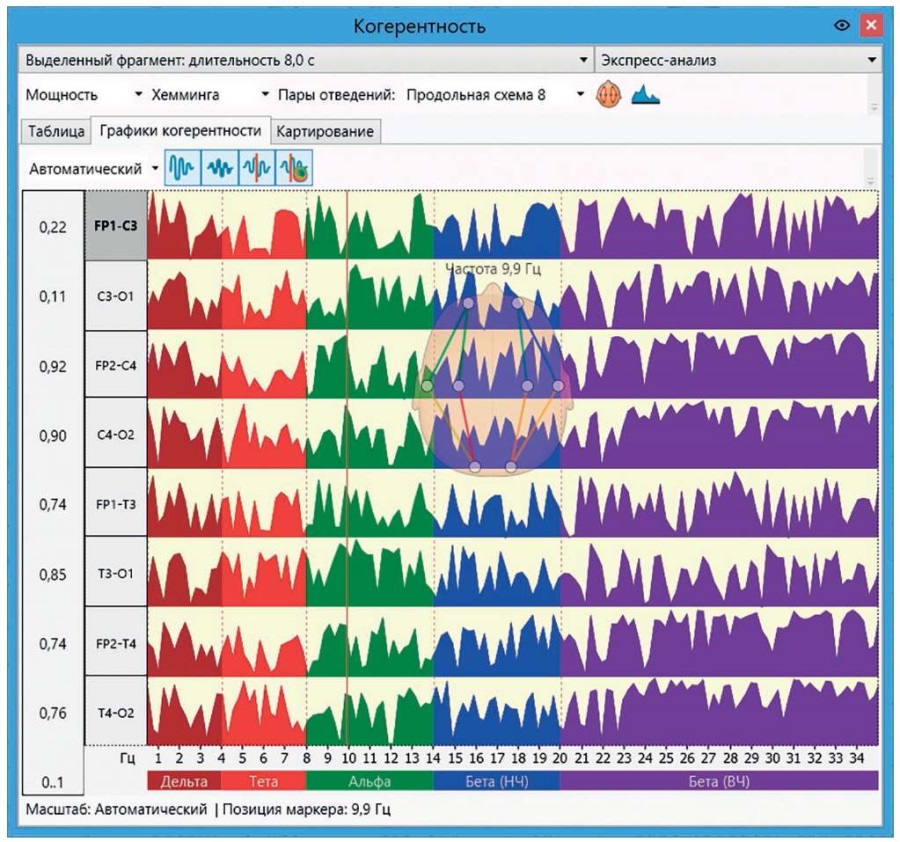
Рисунок 9. Окно с графиками когерентности отображает графики когерентности по каждой паре отведений. По графику можно судить о том, насколько отведения каждой пары коррелируют друг с другом во всем частотном диапазоне и по ритмам
Figure 9. The Coherence Plots window depicts coherence plots for each pair of leads. It allows to judge how the leads in each pair mutually correlate across entire frequency range and rhythms
Периодометрический анализ
Данный вид математического анализа представляет собой некоторую смесь амплитудного и спектрального анализа (но без преобразования Фурье). В ходе периодометрического анализа рассчитываются амплитуда и полупериод каждой ЭЭГ-волны. В результате можно анализировать следующие параметры [13]:
- максимальная амплитуда волн;
- средняя амплитуда волн;
- индекс ритмов волн;
- средние частоты ритмов волн;
- представленность ритмов.
Если с максимальной и средней амплитудой все понятно, то про другие параметры требуется рассказать более подробно. Для расчета индекса ритма рассчитывается отношение количества зарегистрированных волн, попадающих в частотный диапазон данного ритма, к общему количеству зарегистрированных на анализируемом участке волн. Средняя частота ритма вычисляется усреднением средней частоты всех зарегистрированных волн данного ритма. Представленность ритма рассчитывается как отношение количества секунд в анализируемом фрагменте записи, в которые данный ритм зафиксирован, к общему количеству секунд анализируемого фрагмента.
Результаты анализа могут быть представлены в виде таблицы, топографических карт или диаграмм (рис. 10).

Рисунок 10. Окно периодометрического анализа с диаграммами распределения амплитуд и частот. Видно, что наиболее распространенная частота, встречающаяся в анализируемом отрезке, – 10 Гц, а амплитуда – 15 мкВ
Figure 10. Periodometric analysis window with amplitude and frequency distribution. It allows to observe that within the analyzed segment the most common frequency and amplitude are 10 Hz and 15 μV, respectively
Сравнительный анализ
Одним из преимуществ количественного анализа ЭЭГ является возможность объективного сравнения двух участков записи между собой по тому или иному параметру. Для этого можно воспользоваться специальной функцией сравнительного анализа.
Например, она позволяет сравнить фоновую активность ЭЭГ с закрытыми глазами с пробой открывания глаз (рис. 11). Из результатов сравнения видно, что амплитуда альфа-ритма при открывании глаз снизилась на 44,2%, а индекс – на 77,7%, что свидетельствует о депрессии альфа-ритма при открывании глаз, характерной для здорового человека.
С помощью такого инструмента можно сравнить графики спектров, топографические карты и диаграммы как по обоим полушариям, так и по каждому полушарию в отдельности. Также есть возможность сопоставить ЭЭГ-активность в каждом частотном диапазоне по проведенным функциональным пробам (рис. 12).

Рисунок 11. Окно сравнительного анализа. Сравниваются все эпохи пробы «Фоновая запись» с пробой «Открывание глаз». Видна депрессия альфа-ритма на 44,2% и 77,7% по амплитуде и индексу соответственно
Figure 11. A comparative analysis window. All epochs for "Background Recording" vs. "Opening Eyes" tests are compared. The alpha rhythm is depressed by 44.2% and 77.7% in amplitude and index, respectively

Рисунок 12. Сравнение средней амплитуды ЭЭГ по ритмам для проведенных функциональных проб. Из представленного набора топографических карт видно, что средние значения амплитуд достигают своего максимума в дельта-диапазоне в пробах с открыванием и закрыванием глаз. Скорее всего, это связано с наличием артефактов окулограммы, которые следует исключить из эпох анализа
Figure 12. Comparison of the average rhythm-based EEG amplitudes for the performed functional tests. The set of topographic maps allows to observe that the average amplitude magnitude reach the maximum level in the delta range in opening and closing eyes tests. Most likely, it is accounted for by oculogram artifacts, which should be excluded from analysis epochs
Анализ независимых компонент
Одним из современных математических методов удаления артефактов является метод независимых компонент (англ. independent component analysis, ICA) [16]). Этот инструмент позволяет выделить и удалить с кривых ЭЭГ артефакты любого типа. Для эффективной работы данного алгоритма должно быть зарегистрировано достаточное количество ЭЭГ-отведений и артефакт должен по своей форме и структуре отличаться от остальных зарегистрированных сигналов.
В теории, если разместить в одной комнате N чтецов, каждый из которых будет читать свое собственное стихотворение, и не менее N микрофонов, каждый из которых будет записывать смесь звуков от всех чтецов, то с помощью метода независимых компонент из совокупности записей с микрофонов можно выделить звуковые дорожки каждого чтеца в отдельности (независимые компоненты). Если перенести эту модель на ЭЭГ, то мы имеем неизвестное количество источников электрической активности в головном мозге (чтецы) и известное количество ЭЭГ-электродов (микрофоны). Предположим, что количество источников не превышает количество электродов. Тогда можно выделить независимый сигнал от каждого из источников, в т.ч. артефактного.
Еще одним преимуществом данного метода является возможность исключить один или несколько выделенных независимых сигналов и сложить оставшиеся в исходную смесь, лишенную сигналов исключенных источников. Таким образом, метод анализа независимых компонент при некоторых допущениях применим для удаления любых видов артефактов с ЭЭГ-записи. Исключив из ICA-композиции выделенную независимую компоненту, например с электроокулографическим (ЭОГ) артефактом, мы получим тот же самый ЭЭГ-сигнал, но уже очищенный от артефакта (рис. 13).
Важно отметить, что пользоваться данным методом для удаления артефактов следует с осторожностью, т.к. он применим к ЭЭГ только с определенными допущениями и в некоторых случаях при неправильном использовании может привести к искажению исходного ЭЭГ-сигнала.

Рисунок 13. Применение метода анализа независимых компонент (англ. independent component analysis, ICA):
а – пример участка ЭЭГ-записи с электроокулографическими (ЭОГ) артефактами;
b – результат ICA-декомпозиции ЭЭГ-сигнала на 16 независимых компонент (наиболее независимая компонента выведена первой и содержит артефактный ЭОГ-сигнал, полярность сигнала независимой компоненты может отличаться от оригинала);
с – результат обратной ICA-композиции с исключенной компонентой ЭОГ-артефакта позволяет получить очищенную ЭЭГ-запись
Figure 13. Application of the independent component analysis (ICA):
a – a representative EEG recording section with electrooculographic (EOG) artifacts;
b – ICA decomposition of the EEG signal into 16 independent components (the most independent component is highlighted first and contains an artifactual EOG signal, where a signal polarity of the independent component may differ from the original);
c – a reverse ICA composition with the excluded component of the EOG artifact allows to obtain a cleaned EEG record
Анализ трендов
При анализе коротких ЭЭГ-обследований достаточно легко просмотреть все кривые и провести их анализ. Однако при длительных обследованиях просмотр и анализ нативных кривых ЭЭГ может занимать довольно продолжительное время. Для быстрого просмотра количественных показателей длительной ЭЭГ-записи применяются так называемые тренды ЭЭГ. Это результаты расчета определенного параметра, представленные во времени за довольно длительный промежуток.
Например, тренды индексов ритмов волн демонстрируют изменение частотного состава сигнала во времени. Каждый тренд отображает индекс своего ритма. Индекс ритма рассчитывается как отношение площади под графиком спектра в частотном диапазоне этого ритма к общей площади под графиком спектра во всем диапазоне ритмов волн. Индекс ритма выводится в процентах. На панели информации отображаются индексы ритмов волн для текущей позиции на тренде (рис. 14).
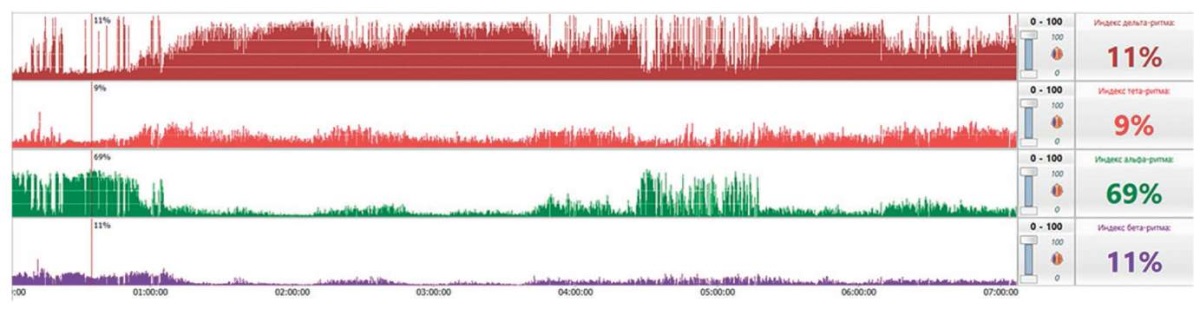
Рисунок 14. Тренды индексов ритмов (сверху вниз): дельта, тета, альфа, бета. По данным трендам довольно легко оценить частотную составляющую сигнала во время продолжительного обследования
Figure 14. Trends of rhythm indices (from top to bottom): delta, theta, alpha, beta. Based on this, it is quite easy to estimate a signal frequency component during a long-lasting examination
Тренд средней амплитуды ЭЭГ показывает рассчитанную среднюю амплитуду волн ЭЭГ по заданным отведениям (по умолчанию в расчете участвуют все видимые отведения текущего монтажа). Такой тренд также называют «огибающей». На панели информации выведена текущая средняя амплитуда волн ЭЭГ в данный момент времени. С помощью элементов управления можно изменить шкалу/масштаб тренда, а также задать уровень значений амплитуды, при котором они будут подсвечиваться красным цветом (рис. 15).
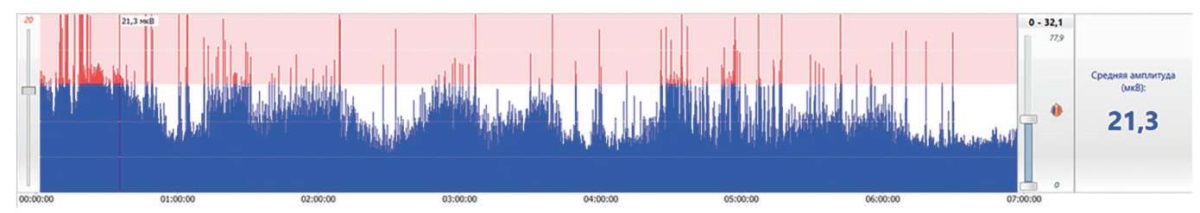
Рисунок 15. Тренд средней амплитуды ЭЭГ
Figure 15. An average EEG amplitude trend
Используя данный тренд, можно легко найти как артефактные участки на длительной записи ЭЭГ, так и спокойные участки, которые можно быстро просмотреть, кликнув на тренде мышкой.
В настоящее время тренды очень широко применяются для количественного анализа ЭЭГ, особенно при мониторинге церебральной функции в палатах интенсивной терапии [17]. Разработаны специализированные программы для расчета и отображения трендов различных показателей ЭЭГ (рис. 16).
При использовании ЭЭГ в палатах интенсивной терапии для оценки функционального состояния центральной нервной системы [17] часто используется тренд амплитудно-интегрированной ЭЭГ.
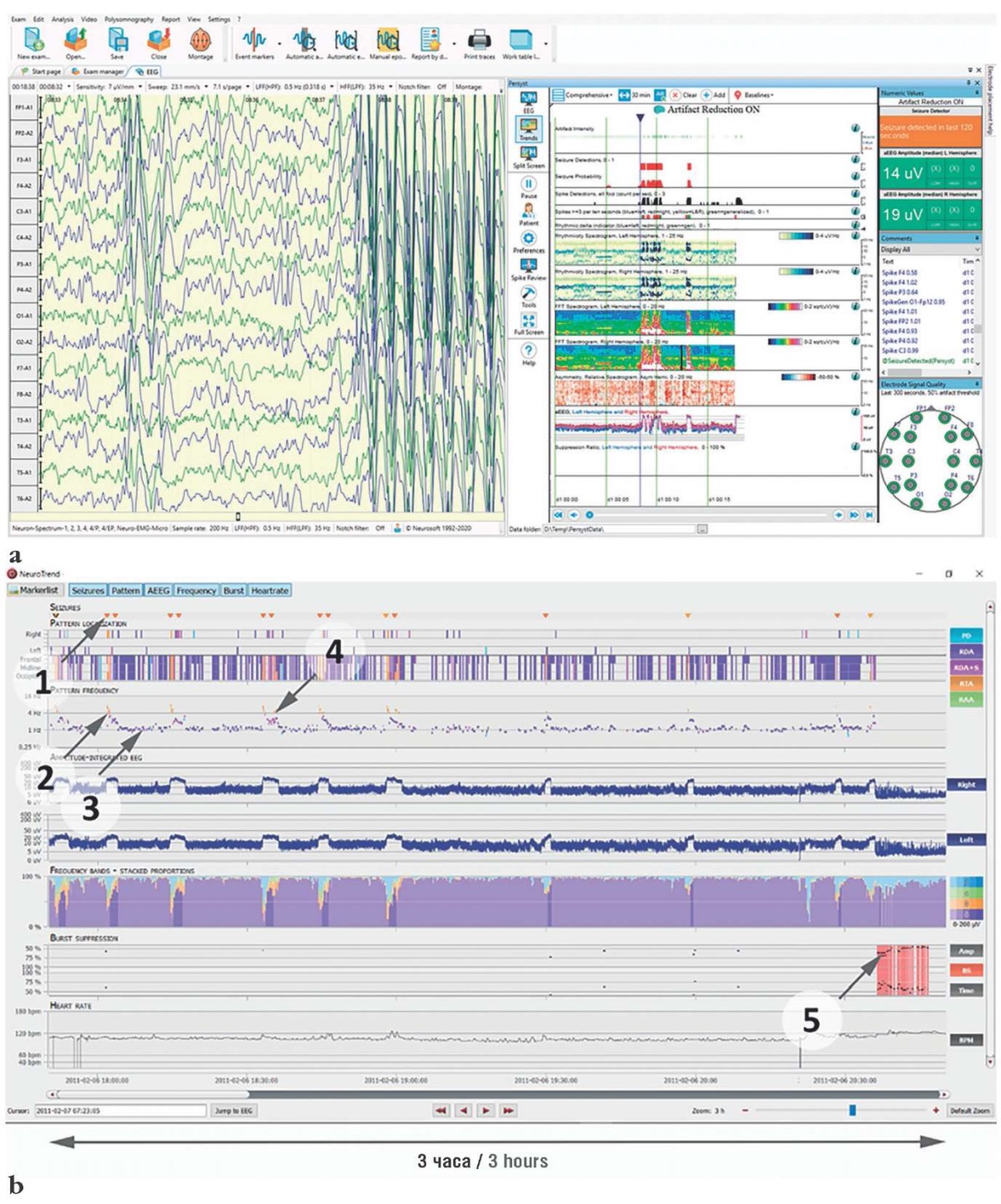
Рисунок 16. Окно трендов ЭЭГ:
а – в программе Persyst v.14 (Persyst Development Corporation Headquarters, США);
b – в программе AIT Encevis Neurotrend (Austrian Institute of Technology, Австрия).
1 – кардиособытия;
2, 3, 4 – тренд представленности медленноволновой активности;
5 – тренд эпизодов «вспышка–подавление»
Figure 16. EEG trend window:
a – assessed in Persyst v.14 (Persyst Development Corporation Headquarters, USA);
b – assessed in AIT Encevis Neurotrend (Austrian Institute of Technology, Austria).
1 – cardio events;
2, 3, 4 – trend for representation of slow-wave activity;
5 – trend for burst-suppression episodes
Вейвлет-анализ
При просмотре ЭЭГ на экране в виде кривых мы видим амплитудно-временное представление сигналов головного мозга обследуемого. Такое представление данных не всегда является наилучшим. Зачастую полезная информация скрыта в частотной области сигнала. Для получения информации о частотной составляющей сигнала используется преобразование Фурье. В результате такого преобразования заданного во временной области сигнала получается его спектральное представление.
Однако преобразование Фурье говорит лишь о том, каково содержание каждой частоты в сигнале, но остается неизвестным, в какой момент времени доминирует та или иная частота. Для локализации во времени спектральных компонентов сигнала как раз и служит вейвлет-преобразование, которое позволяет получить частотно-временное представление сигнала (рис. 17а). Такой же график вейвлет-анализа можно получить и в трехмерном виде (рис. 17b), это позволит не только оценить частотный состав сигнала, но и отследить, в какие моменты времени в сигнале преобладали те или иные частоты.

Рисунок 17. Результаты вейвлет-анализа ЭЭГ:
а – частотно-временное отображение ЭЭГ-сигнала;
b – трехмерное представление результатов вейвлет-преобразования
Figure 17. EEG wavelet analysis:
a – time-frequency display of EEG signal;
b – three-dimensional representation of wavelet transform data
Инструменты автоматического поиска на ЭЭГ / Automatic EEG search tools
Кроме инструментов для количественного анализа важную роль в современных программах обработки ЭЭГ играют алгоритмы автоматического поиска различных феноменов:
- артефактов записи;
- спайков и острых волн;
- эпизодов пароксизмальной активности;
- эпизодов «вспышка – подавление».
Использование подобных инструментов существенно ускоряет просмотр и анализ длительных ЭЭГ-записей.
Специализированные программы для количественного анализа ЭЭГ / Specialized programs for quantitative EEG analysis
Благодаря тому, что запись ЭЭГ в результате количественной обработки может быть представлена в виде набора цифр (количественная ЭЭГ), можно сравнить ЭЭГ-записи разных людей. Также это позволяет создать базы данных параметров ЭЭГ, включающие как здоровых людей, так и пациентов с различными нарушениями.
Таким образом, появится возможность сравнить любую запись ЭЭГ (вернее, ее количественное представление) с существующими базами норм и сделать вывод о нормальности или ненормальности конкретной ЭЭГ. Разработки в этом направлении продолжаются в настоящее время, но некоторые коммерческие пакеты программ для подобного сравнения уже представлены. Ниже перечислены некоторые из них.
iSyncBrain
Южнокорейская система для сравнения количественной ЭЭГ с нормативной базой данных iSyncBrain v.3.0 предлагает веб-интерфейс, личный кабинет и возможность загрузки ЭЭГ-записей для расчета количественных показателей и их сравнения с нормативными значениями (рис. 18).

Рисунок 18. Программа iSynchBrain v.3.0 (Южная Корея) предлагает довольно богатый набор расчетных параметров для сравнения с возрастными нормами ЭЭГ (частотная представленность, индексы ритмов волн, амплитудные параметры, топографическое картирование, расчет корреляции)
Figure 18. iSynchBrain v.3.0 (South Korea) software allows to comprehensively assess calculated parameters for comparing with EEG age-related normal range (frequency representation, wave rhythm indices, amplitude parameters, topographic mapping, correlation calculation)
Epilog PreOpp
Система для количественного анализа ЭЭГ и сравнения результатов с нормативной базой данных Epilog
Pre Opp (EEG Diagnostic Technology, Бельгия) представлена на рисунке 19. Данный программный пакет также позволяет провести обсчет нативной ЭЭГ, сравнить результаты с базой норм и подготовить отчет.
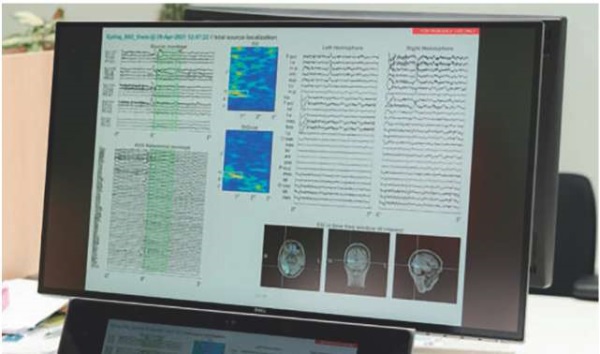
Рисунок 19. Интерфейс программы Epilog Pre Opp (EEG Diagnostic Technology, Бельгия)
Figure 19. Interface of the Epilog Pre Opp (EEG Diagnostic Technology, Belgium) software
QEEG Pro
Загрузив данные ЭЭГ в систему для обработки ЭЭГ через веб-интерфейс QEEG Pro (qEEG-Pro, Нидерланды), пользователь получает возможность их сравнения между собой по нескольким расчетным параметрам (рис. 20).

Рисунок 20. Программа QEEG Pro (qEEG-Pro, Нидерланды)
Figure 20. QEEG Pro (qEEG-Pro, Netherlands) software
NeuroGuide
Программный пакет NeuroGuide (Applied NeuroScience, США) с широким функционалом по обработке и анализу ЭЭГ предоставляет богатый набор инструментов для количественного анализа ЭЭГ, включая их сравнение с базой норм (рис. 21).
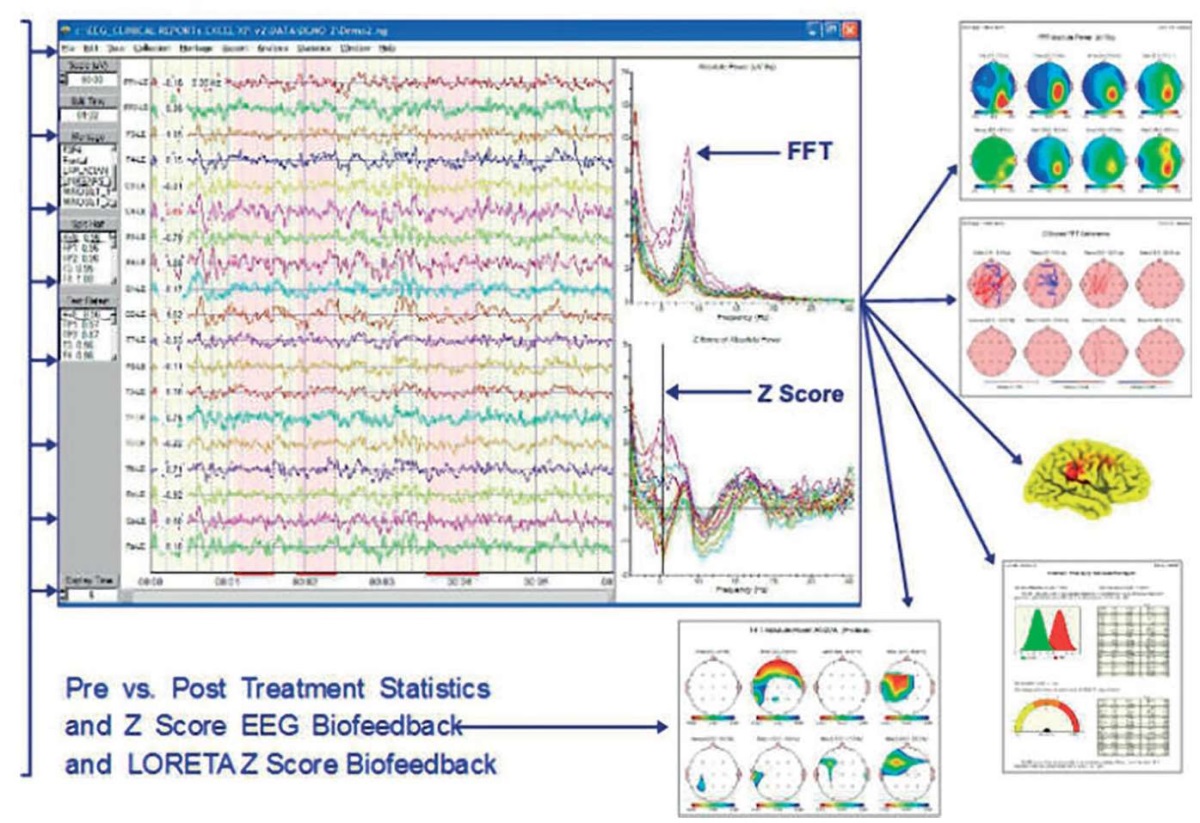
Рисунок 21. Функционал программы NeuroGuide (Applied NeuroScience, США)
Figure 21. Features of NeuroGuide (Applied NeuroScience, USA) software
BrainLoc
Российский программный продукт BrainLoc v.6.0 предназначен для трехмерной локализации источников патологической активности в головном мозге по ЭЭГ (рис. 22).
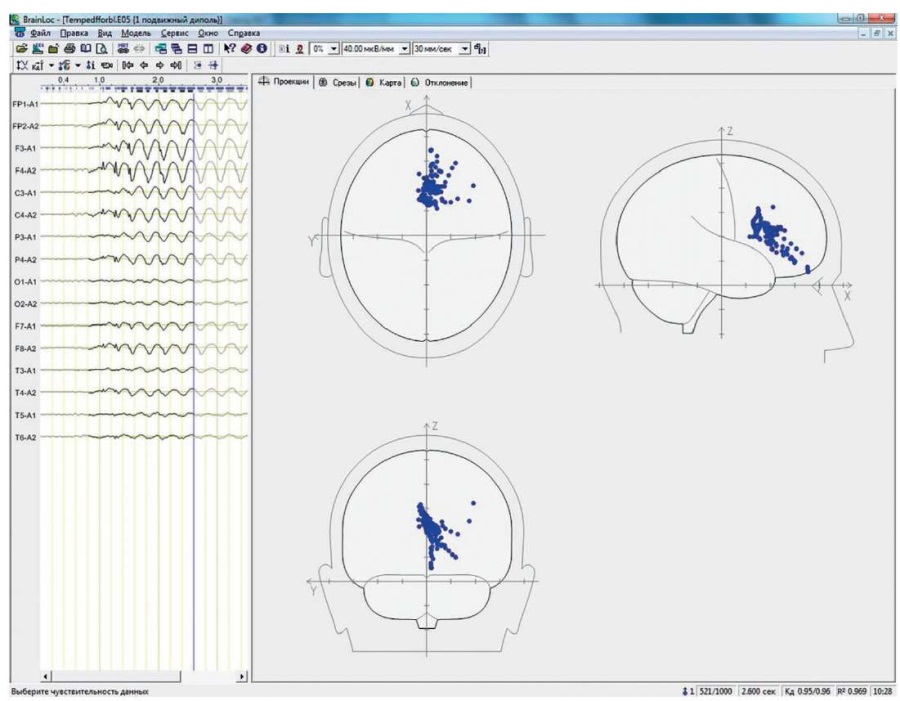
Рисунок 22. Программа BrainLoc 6.0 (Россия) позволяет вычислить локализацию источников патологической активности в головном мозге по загруженному участку ЭЭГ-кривых
Figure 22. BrainLoc 6.0 (Russia) software allows to calculate localization of pathological activity sources in the brain based on uploaded EEG curve section
Brainsys-bank
Отечественный программный продукт Brainsys-bank v.6.0 позволяет сопоставлять спектральные параметры ЭЭГ (абсолютная мощность, относительная мощность, когерентность и др.) с нейрометрическим банком ЭЭГ-данных (рис. 23).

Рисунок 23. Программа Brainsys-bank (Россия) для сопоставления спектральных параметров ЭЭГ с нейрометрическим банком ЭЭГ-данных
Figure 23. Brainsys-bank (Russia) software to align EEG spectral parameters with neurometric EEG database
Для сравнения с нейрометрическим банком вычисляются спектральные параметры ЭЭГ и затем преобразуются к нормальному распределению Гаусса. Нейрометрический банк получен из нормативной базы ЭЭГ здоровых лиц и содержит статистические характеристики: среднее и стандартное отклонение (англ. standard deviation, SD) для данной группы определенного возраста и пола. Сравнение с нормативными ЭЭГ-данными проводится при помощи Z-критерия, в котором величина Z, определенная как степень отклонения от среднего по нормативной группе в единицах стандартного отклонения, не должна в норме превышать 2–3 SD. Подобный анализ ЭЭГ, позволяющий сопоставить данные каждого пациента с его возрастной нормой и оценить степень и характер отклонений от нормативных данных, в значительной степени способствует правильной диагностике заболевания.
Известно, что ЭЭГ очень быстро меняется в детском возрасте, поэтому ЭЭГ-данные в банке сгруппированы с шагом в полгода для возраста от 3 до 17 лет. Взрослые сгруппированы с шагом 2,5 года от 18 до 80 лет.
Нормативная база ЭЭГ собрана сотрудниками ФГБНУ «Научный центр психического здоровья», Московского научно-исследовательского института психиатрии – филиала ФГБУ «Федеральный медицинский исследовательский центр психиатрии и наркологии им. В.П. Сербского» Минздрава России, ФГАОУ ВО Российский национальный исследовательский медицинский университет имени Н.И. Пирогова» Минздрава России, ФГБУН «Институт высшей нервной деятельности и нейрофизиологии» Российской академии наук, а также других организаций.
LORETA
Швейцарская программа LORETA v.1994 (англ. low-resolution brain electromagnetic tomography) для обработки результатов электромагнитной томографии головного мозга с низким разрешением широко применяется в научных исследованиях (рис. 24).
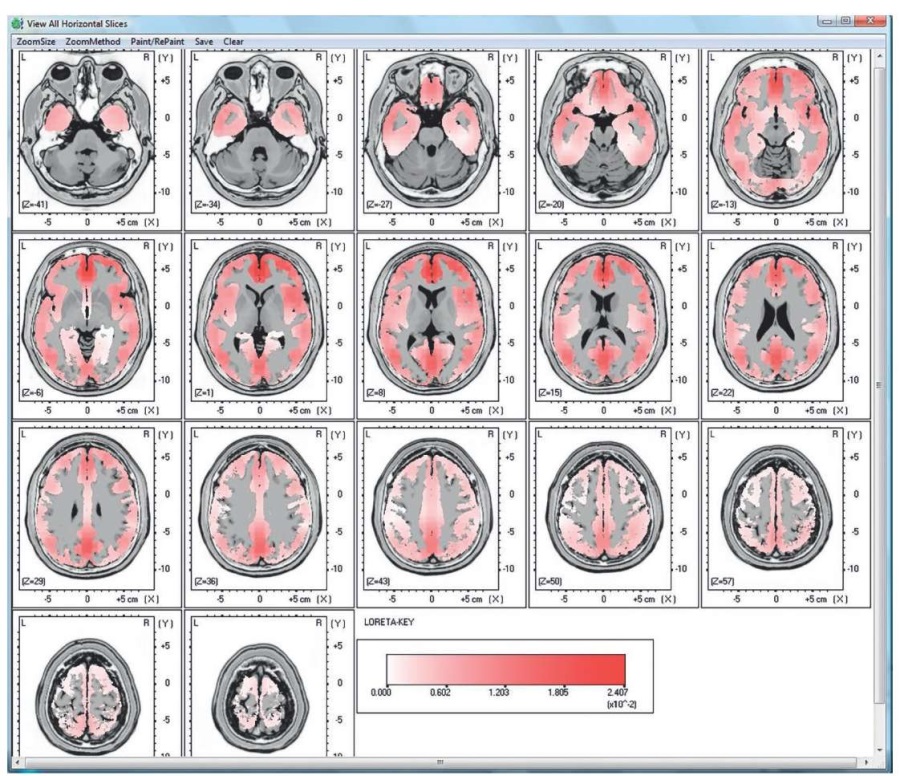
Рисунок 24. Программа LORETA (Швейцария)
Figure 24. LORETA (Switzerland) software
BESA v.2.0
Немецкий пакет программ широкого назначения BESA (англ. Brain Electrical Source Analysis) также используется для обработки и анализа ЭЭГ (рис. 25).

Рисунок 25. Программа BESA (Германия)
Figure 25. BESA (Germany) software
Экзотические виды анализа ЭЭГ / Exotic types of EEG analysis
Вышеперечисленные виды математического анализа ЭЭГ-сигналов применяются довольно часто и являются в большей степени общепризнанными. Но есть и такие математические приемы, которые в настоящее время используются только в научных исследованиях.
Степень сжатия по Лемпелю–Зиву
Алгоритм Лемпеля–Зива – один из первых алгоритмов сжатия информации. Он сжимает информацию тем лучше, чем больше в исходном сигнале повторяющихся комбинаций. К примеру, если в исходном сигнале повторяется всего один символ, то степень сжатия будет максимальной, а если, наоборот, ни один символ в последовательности не повторяется, то степень сжатия будет минимальной.
Исследователи попробовали применить этот алгоритм сжатия к сигналу ЭЭГ и получили интересные результаты. Поскольку степень сжатия по Лемпелю–Зиву характеризует повторяемость сигнала, то чем повторяемость сигнала лучше, тем степень сжатия выше. Для здорового человека этот показатель при сжатии ЭЭГ может колебаться от 60% до 90%, а, например, при болезни Альцгеймера и других расстройствах функционирования головного мозга он может снижаться до 40%, т.к. ЭЭГ-сигнал у таких больных более разнообразен и хуже воспроизводится (отсутствует ритмика, автокорреляция снижена). Наблюдая за изменением данного показателя во времени, можно отслеживать динамику хода лечения или развития заболевания.
Mathlab, EEGLab, Simulink, OpenVibe
Для экзотической математической обработки ЭЭГ-сигнала в научных исследованиях, как правило, применяются такие специализированные программные пакеты, как MathLab, EEGLab, Simulink (США), OpenVibe (Франция). С их помощью исследователь может самостоятельно запрограммировать операции, выполняемые над ЭЭГ-сигналом. Для экспорта ЭЭГ-данных в указанные математические пакеты обычно применяется формат EDF+ (англ. European Data Format) или протокол LSL (англ. Lab Stream Layer).
ЗАКЛЮЧЕНИЕ / CONCLUSION
С помощью современных способов математической обработки и анализа ЭЭГ данный метод исследования становится более информативным и объективным. Большинство перечисленных в статье инструментов количественного анализа ЭЭГ применимо в клинической практике при условии, что пользователь разбирается в принципах работы каждого алгоритма. Некоторые из приведенных инструментов пока применяются только в научных исследованиях, но могут также использоваться и в клинической практике, расширяя возможности традиционного визуального анализа ЭЭГ-сигналов.
Еще раз подчеркнем, что современные методы математической обработки сигнала для анализа ЭЭГ необходимо применять только при понимании принципов их работы и ограничений, которые они имеют. Не следует целиком и полностью полагаться на автоматизированные инструменты: они предоставляют лишь дополнительные средства для оценки, помогая ускорить ее, но никак не заменяют мнение врача, проводящего анализ ЭЭГ-обследования.
Список литературы
1. Иванов А.А. Телемедицинские решения для инструментальной диагностики на дому у пациента в условиях пандемии. Журнал телемедицины и цифрового здравоохранения. 2021; 7 (1): 25–34. https://doi.org/10.29188/2542-2413-2021-7-1-25-34.
2. Иванов А.А. Устройство современного электроэнцефалографа. Эпилепсия и пароксизмальные состояния. 2022; 14 (4): 362–78. https://doi.org/10.17749/2077-8333/epi.par.con.2022.138.
3. Иванов А.А. Обзор возможностей современного программного обеспечения для регистрации и анализа ЭЭГ. Эпилепсия и пароксизмальные состояния. 2023; 15 (1): 53–69. https://doi.org/10.17749/2077-8333/epi.par.con.2023.144.
4. Рекомендации экспертного совета по нейрофизиологии Российской Противоэпилептической Лиги по проведению рутинной ЭЭГ. Эпилепсия и пароксизмальные состояния. 2016; 8 (4): 99–108.
5. Методические рекомендации «Методика регистрации и формирования заключения по ЭЭГ». Департамент здравоохранения города Москвы, 2021. URL: https://neurosoft.com/files/catalog/catalog/753/ru/files/Metodika-registracii-i-formirovaniyazaklyucheniya-po-EEG--Moskva--2021.pdf (дата обращения 29.11.2022).
6. Sinha S.R., Sullivan L., Sabau D., et al. American Clinical Neurophysiology Society Guideline 1: minimum technical requirements for performing clinical electroencephalography. J Clin Neurophysiol. 2016; 33 (4): 303–7. https://doi.org/10.1097/WNP.0000000000000308.
7. Peltola M.E., Leitinger M., Halford J.J., et al. Routine and sleep EEG: minimum recording standards of the International Federation of Clinical Neurophysiology and the International League Against Epilepsy. Clin Neurophysiol. 2023; 147: 108–20. https://doi.org/10.1016/j.clinph.2023.01.002.
8. Якимов Е.В. Цифровая обработка сигналов. 2-е изд. Томск: Издательство Томского политехнического университета; 2011: 168 с. URL: https://portal.tpu.ru/SHARED/s/SOCRAT1975/eng/academics/Tab/DSP_Textbook_2011.pdf (дата обращения 29.11.2022).
9. Tatum W.O., Mani J., Jin K., et al. Minimum standards for inpatient long-term video-EEG monitoring: a clinical practice guideline of the International League Against Epilepsy and International Federation of Clinical Neurophysiology. Clin Neurophysiol. 2022; 134: 111–28. https://doi.org/10.1016/j.clinph.2021.07.016.
10. Поворинский А.Г., Заболотных В.А. Пособие по клинической электроэнцефалографии. Л.: Наука; 1987: 64 с.
11. Зенков Л.Р. Клиническая энцефалография (с элементами эпилептологии). 8-е изд. М.: МЕДпресс-информ; 2017: 360 с. URL: https://static-eu.insales.ru/files/1/6854/3136198/original/klinich_electroenzefalografija.pdf (дата обращения 29.11.2022).
12. Александров М.В. (ред.) Электроэнцефалография. СПб.: СпецЛит; 2020: 224 c.
13. Кулаичев А.П. Компьютерная электрофизиология и функциональная диагностика. 4-е изд. М.: Форум; 2007: 639 с.
14. Jasper H.H. The ten-twenty electrode system of the International Federation. Electroencephalogr Clin Neurophysiol. 1958; 10: 371–5.
15. Seeck M., Koessler L., Bast T., et al. The standardized EEG electrode array of the IFCN. Clin Neurophysiol. 2017; 128 (10): 2070–7. https://doi.org/10.1016/j.clinph.2017.06.254.
16. Kropotov J.D. Quantitative EEG, event-related potentials and neurotherapy. 1st ed. Academic Press; 2010: 924 pp.
17. Синкин М.В., Баранова Е.А. (ред.) Электроэнцефалография у пациентов с нарушением сознания. Методология описания и клинические примеры. М.: Атмосфера; 2022: 88 с.
Об авторе
А. А. ИвановРоссия
Иванов Алексей Алексеевич – руководитель отдела управления продуктами
ул. Воронина, д. 5, Иваново 153032
Рецензия
Для цитирования:
Иванов А.А. Обзор методов математического анализа ЭЭГ. Количественная ЭЭГ. Эпилепсия и пароксизмальные состояния. 2023;15(2):171–192. https://doi.org/10.17749/2077-8333/epi.par.con.2023.154
For citation:
Ivanov А.А. Overview of mathematical EEG analysis. Quantitative EEG. Epilepsy and paroxysmal conditions. 2023;15(2):171–192. (In Russ.) https://doi.org/10.17749/2077-8333/epi.par.con.2023.154

Контент доступен под лицензией Creative Commons Attribution-NonCommercial-ShareAlike 4.0 International License.










































